|
1Заслуженный профессор физики твердого тела и директор-основатель лаборатории материаловедения Университета штата Пенсильвания (rroy@psu.edu); 2Заслуженный профессор и бывший зав. кафедрой материаловедения Стэнфордского университета; 3Профессор медицины, психиатрии, семейной и общественной медицины, здравоохранения, директор программы исследований по интегративной медицине, Аризонский университет (ibell@u.arizona.edu); 4Доцент НИИ материаловедения Университета штата Пенсильвания (rickhoover@psu.edu)
Оригинал можно скачать здесь
©2005 Matrice Technology Limited
Данная статья дает междисциплинарную базу информации по структуре жидкой воды. Она начинается с обобщения имеющейся в литературе по материаловедению информации о структуре1 аморфной неорганической ковалентной жидкой фазы, примеры которой мы видим в SiO2, S, Se, P и H2O. Данные по воде проанализированы через призму известных алгоритмов материаловедения: связь свойств со структурой, фазовые диаграммы температура-давление (P–T), явление эпитаксии, явление разделения фаз жидкость-жидкость, стабильность двухфазных коллоидов, недавно обнаруженное действие слабых магнитных и электрических полей на структуру простых неорганических оксидов. Другую обширную базу данных дало тщательное изучение литературы о свойствах конденсированного вещества, отражающей структурные особенности практически чистой воды, получаемой в процессе обычной технологии приготовления гомеопатических средств.
Проверка этих данных при помощи стандартных парадигм материаловедения приводит к следующему заключению: для опытов и процессов при условиях, близких к нормальным, должносуществовать множество различных структур жидкой воды. Типичный образец воды в таких экспериментальных условиях, без сомнения, состоит из определяемого статмеханикой комплекса мономеров и олигомеров (кластеров) различных размеров — по крайней мере, до сотен молекул H2O. Структурное подобие SiO2 и OH2 очень важно как для структуры воды, так и для возможности эпитаксии по крайней мере в области контакта со стеклянными стенками обычных сосудов.
Главная отличительная особенность связей в жидкой воде это не только "хорошо известные водородные связи, но обязательное наличие широкого спектра" связей Ван-дер-Ваальса между различными олигомерными (кластерными) структурными элементами. Это тот диапазон очень слабых связей, который может отвечать за поразительную легкость изменения структуры воды, которая, в свою очередь, может помочь объяснить полдюжины известных аномалий ее свойств. В наиболее тонкой форме такие слабые связи могли бы давать изменения структуры, вызванные электрическими и магнитными полями и излучениями всех типов, включая, возможно, так называемые "тонкие энергии", на которых основано огромное число заявлений об особенным образом "структурированной" воде.
Эта работа ни в коем случае не касается клинической эффективности какого-либо гомеопатического средства. Однако она, несомненно, опровергает довод против гомеопатии, который основан на совершенно ложном утверждении, что если нет различий по составу между лекарством и использованной для него чистой водой, то между ними вообще не может быть различий. Мы показываем несостоятельность подобного утверждения с помощью главной парадигмы материаловедения, заключающейся в том, что структура (а не состав) в значительной степени управляет свойствами, и структуры в неорганических фазах могут быть легко изменены без какого-либо изменения состава. Таким образом, критики гомеопатии должны доказать идентичность структуры приготовленного средства и исходного растворителя.
Основные выводы данной работы касаются только правдоподобности биологического действия высокоразведенных водных лекарств; выводы эти основаны на очень старых (гомеопатия) и недавних (металлические и нанопузырьковые коллоиды) наблюдениях, которые были отвергнуты без должных оснований или из-за незнакомства с литературой по материаловедению и с его теоретическим фундаментом. Это превосходный пример частой ошибки при неприятии новых научных открытий, когда отсутствие доказательства считается доказательством отсутствия.
Ключевые слова: вода, структура воды, эпитаксия, нанопузыри, коллоиды.
Введение
По запросу "структура жидкой воды" "Гугль" выдает примерно 8 миллионов ссылок, а по запросу "структура воды" в два раза больше. Любое дополнение в эту обширную массу знаний едва ли будет существенным. В настоящей работе не сообщается ни о неуклонном прогрессе в ультрапрецизионных измерениях структуры олигомеров, ни о фемтосекундной спектроскопии разрыва связей или фазовых переходах в стекловидной воде (это аморфное состояние, которое обычно получается, когда скорость охлаждения намного превышает скорость кристаллизации. — прим. ред.). Вместо этого мы анализируем литературные данные, чтобы обосновать только одно утверждение — чистая, термодинамически устойчивая или метастабильная жидкая вода может иметь более одной трехмерной (3-D) структуры. Хотя мы приводим здесь разные данные и доказательства этого, так совпало, что когда эта работа была представлена впервые (апрель 2004 г.), Кавамото и др. опубликовали свою работу с экспериментальными доказательствами этого утверждения [1, 2]. Конечно, было известно, что в твердой кристаллической воде существует около 10 различных структур, и такие ученые, как Анджелл, Де Бенедетти и Стэнли дали чрезвычайно точную и интересную картину по некоторым метастабильным состояниям жидкой воды или метастабильным твердым водяным стеклам с различными свойствами и структурой [3, 4]. Эти наблюдения заставляют вспомнить о тех же самых явлениях, которые известны в течение поколений для SiO2, близкого родственника H2O. Эта работа сводит воедино совершенно разные исследования по воде (и другим жидкостям, имеющим один или более параметр структуры или связи), чтобы подтвердить факт, что вода действительно может весьма легко нелинейным образом менять свои свойства и, соответственно, структуру, без какого-либо изменения состава.
Структура кристаллического неорганического вещества, которая стала главной основой физики и химии твердого тела, основывалась на открытии фон Лауэ и Браггов, отца и сына, дифракции рентгеновского излучения периодичной решеткой атомов в кристаллических твердых телах. Она остается обязательной для характеристики веществ в современном материаловедении. За Браггсами последовали школы В. М. Голдшмидта (включая Барта, Лунде и Захариасена в Осло), и Лайнуса Полинга в Калифорнии, которые применили новый метод рентгеновской дифракции (XRD) к большому числу неорганических твердых веществ (кристаллов), широко используемых в неорганической химии и технологии. Так родилась чрезвычайно точная наука кристаллохимия, изучающая связь строения и состава как функции термодинамических переменных, температуры и давления (см. книги Голдшмидта, Полинга, Эванса, Мюллера и Роя [5–8]). В кристаллохимии термин структура однозначно определяется трехмерными координатами каждого атома или иона с точностью, составляющей в настоящее время порядка 0,01 нм.
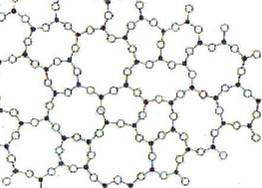
Что сразу привлекает внимание в учебнике по неорганической кристаллохимии заинтересованного наблюдателя, это соотношение объема материала по твердым веществам и по жидкостям. Оно приближается к 100:1, и это не шутка. Почему? Вода в виде жидкости — наиболее распространенная фаза на поверхности Земли, за которой следует лед. С большим отрывом на втором месте идет кристаллический SiO2 в виде кварца (одна из дюжины различающихся структурных форм SiO2). Тот факт, что мы знаем мельчайшие подробности строения каждой формы кристаллического SiO2 и при этом имеем только зачаточные представления о жидком SiO2 — следствие фундаментального пробела в нашем арсенале инструментов для определения структуры жидкостей. Сложность состоит не в том, что в маловязких жидкостях происходит непрерывное быстрое движение содержащихся в ней атомов и/или молекул. Такой эффективный инструмент, как XRD, совершенно непригоден для всех некристаллических (т.е. апериодических) веществ, твердых или жидких. Единственный инструмент, который сегодня можно использовать с уверенностью и напрямую (хотя и частично) для определения структуры некристаллических твердых веществ (например, стекол), это просвечивающий электронный микроскоп (TEM), но и он с трудом может быть использован для жидкостей напрямую. Неудивительно, что многие ученые, вследствие невежества или отсутствия нужного оборудования, придерживаются наивного взгляда, что жидкости, подобно большинству кристаллов, более или менее полностью структурно гомогенны вплоть до атомарного или молекулярного уровня, и рассматривают структурные характеристики в соответствии с моделью случайной сетки, одной из двух разработанных около века назад моделей для стекол. В этой модели "структуры стекла" рассматривают структурно гомогенное кристаллическое вещества (т.е. у которого структурный элемент, элементарная ячейка, повторяется в образце по всем трем измерениям), а затем смещают атомы или ионы из их нормального положения, задаваемого периодичностью, путем изгиба либо растяжения связей. На рис. 1 показана заимствованная из оригинальной работы Захариасена [9] эта так называемая модель случайной сетки2:
| |
 |
|
Рис. 1 Классическая картинка "структуры случайной сетки", предложенная Захариасеном в 1932 г., которая стала "общепринятой" для строения стекла на основе модели, подобранной по данным рентгенографии. Ключевое допущение этой модели (не понятое другими исследователями в течение семи или восьми десятилетий), что структура всех стекол "гомогенна" в той же степени, как у кристаллов.
|
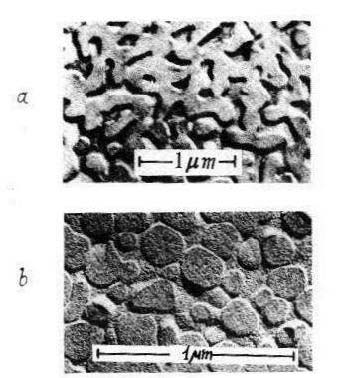
Эта устаревшая на сегодняшний день картинка, не основанная ни на каких прямых данных, полученных другими методами, с тех пор всегда доминировала в представлениях физиков и химиков и стала их "рабочей моделью". Оппонентом данной "гомогенной структуры" выступала более ранняя "кристаллитная" теория Принса, согласно которой небольшие (5-50 Å) фрагменты различных кристаллических структур плавают в окружении мономеров [10]. В течение более полувека на международных конференциях периодически поднимался вопрос о гомогенной (случайная сетка) и гетерогенной (кристаллиты) структуре стекол (замороженных жидкостей). В 1980-х решающие данные были получены посредством не XRD, а TEM обычных щелочных боро- и алюмосиликатных стекол (Мазурин и Порай-Кошиц; рис. 2 взят из их работы), которая показала гетерогенную "наноструктуру" для очень многих прозрачных стекол, в которой имелись две или четыре различные фазы [11] (фазы определялись как области с характерной структурой или составом, разделенные границей)!!
| |
 |
|
Рис. 2 Резкий контраст между гипотетическими расчетами, основанными на теории случайной сетки Захариасена, и непосредственными данными, полученными с помощью TEM. Приведены примеры двойных и тройных стекол — некоторые закаленные, некоторые термообработанные — отчетливо демонстрирующие реальное разделение фаз. Можно с уверенностью предположить, что во многих, если не в большинстве стекол и во многих жидкостях должны существовать структурные флуктуации как прекурсоры такого разделения фаз (согласно Мазурину и Порай-Кошицу) [11].
|
Существование целой стеклокерамической промышленности зависит от этих зарождающейся наногетерогенности или реального разделения фаз в стекле, и несметное число TEM-изображений от Корнинга (Беалл и Пинкни) показывает настоящие нанокомпозиты [12]. Наличие или высокая вероятность наногетерогенности структуры в большинстве стекол и жидкостей с прочными связями признана сегодня в качестве "стандартной модели".
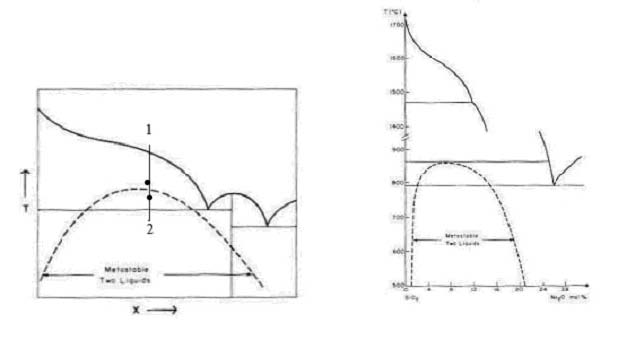
В 1960 г. Рой привел термодинамические доводы для использования метастабильной несмешиваемости как индикатора вероятной наногетерогенности в материнских жидкостях [13]. Реальная несмешиваемость — более поздняя стадия развития гетерогенности, жидкости проявляют свою зачаточную гетерогенность реальным разделением на различные фазы в переохлажденном состоянии (см. рис. 3). Структура жидкости в точке 1, как можно заключить, должна иметь зачаточную гетерогенность или области или кластеры в начальной фазе разделения, которые реально формируются, скажем, в точке 2. Термодинамика неидеальной формы ликвидуса служит индикатором возможного разделения фаз (разумеется, это относится к двухкомпонентной системе и это проще представить).
| |
 |
|
Рис. 3 Первая презентация Роем (1960) теоретического вывода, что неидеальность ликвидуса (ясно показываемая его формой) говорит о том, что сама жидкая фаза "гетерогенна" по структуре, и можно вызвать разделение фаз в той области температур, где она метастабильна (рисунок слева) [13]. Порай-Кошиц и Аверьянов экспериментально продемонстрировали в точности такой же пример в 1968 г. [14]
|
Неизбежная "тенденция" к неоднородности с тех пор была сильно развита и полностью доказана на сотнях случаев (смотри полное изложение Мазурина и Порай-Кошица [11, 15]. Сегодня существуют обширные и точные экспериментальные доказательства высокой гетерогенности нано- и микроструктур, даже для множества отдельных областей, и в т.ч. для фаз Гиббса по крайней мере в сотнях обычных закаленных жидкостях и стеклах.
Важное наблюдение о возможной структуре воды, кинетике разрыва связей и т.д., и их соответствие структуре может быть сделано из фазовой диаграммы на рис. 3. В верхней части метастабильной двухжидкостной области на фазовой диаграмме слева наблюдается "критическая точка раствора". Прежде всего отметим, что взаимодействие фаз, включающее критические точки в несмешивающихся жидкостях, достаточно распространено в простых бинарных системах с водой, классические примеры — фенол + вода, никотин + вода и т.д., детально рассмотренные Риччи в его учебнике по правилу фаз [16]. Непосредственно выше критической температуры мы имеем одну фазу; ниже — две фазы, бесконечно мало отличающиеся по составу. Поэтому ниже критической температуры совершенно очевидно существование двух фаз с различными структурами, которые стабильны вместе "навсегда". Теперь рассмотрим, что изменится, когда мы поднимем температуру на бесконечно малую величину выше критической температуры. В контексте данной статьи логично предположить, что структура этой жидкости наногетерогенна и содержит области — кластеры или "олигомеры" — соответствующие разным структурам, которые формируются при температуре всего на один градус Цельсия ниже критической. Это доказывает гладкий непрерывный наклон кривой ликвидуса при сильно неидеальной форме.
Переходя от возможной наногетерогенности структуры к кинетике, рассмотрим утверждение, что "быстрый разрыв и восстановление связей" исключает возможность сосуществования различных структур в жидкой воде. Можно уверенно предположить, что такая кинетика не изменится просто потому, что разделение фаз может происходить при практически постоянной температуре. Очевидно, эта очень быстрая кинетика разрушения и восстановления связей не имеет значения, т.к. она имеет место в пределах каждой структурной конструкции элементов без статистического влияния на структуру самих элементов.
По давней традиции в классической химии и материаловедении предполагалось и со временем стало каноном, что жидкости с постоянным составом не содержат двух фаз. Это предположение было опровергнуто экспериментально в 1970–х гг. Тогда было показано, что в пространстве P—T (давления-температуры) даже в области стабильной жидкости (а не только в метастабильных стеклах) можно найти множество различных структур — напримеро, в расплавах оксидов и даже в таких одноатомных системах, как элементарные S, Se и Те [17–19]. Рис. 4 показывает взятую из этих работ фазовую диаграмму S с отчетливыми фазовыми областями для нескольких отличающихся жидкостей. На жаргоне двух последующих десятилетий работ по полиаморфизма H2O-стекла, это полиаморфизм стабильной жидкости S, Se и Те. Далее мы покажем (рис. 6), как этот важный вывод может быть специфически распространен на саму H2O.
| |
 |
|
Рис. 4 Р-Т фазовая диаграмма для серы (S). Слева — область ниже ликвидуса, на которой показано множество кристаллических структур. Справа — область стабильной жидкости, в которой наблюдаются по меньшей мере 5 различных жидких структур, разделенных фазовыми границами.
|
На рис. 4 левая картинка показывает P—T фазовые диаграммы для серы с 12 кристаллическими фазами, взятые у Веццоли и др. [17] Отметим четкие разрывы в ликвидусе. На правой картинке из работы тех же авторов показана фазовая диаграмма области стабильной жидкости [20]. В то время (1969) считалось, что возможна только одна жидкая фаза. Тем не менее, авторы вероятно впервые представили экспериментальное доказательство различно структурированных жидких фаз A, B, C, D, E, разделенных несколько нечеткими (второго порядка?) границами P-T. Другим подходящим примером, хотя и метастабильным, является стекловидный углерод. Изучение с помощью TEM (рис. 5) показывает, что в стекловидном углероде смыкающиеся области из sp2-графита размером 1–2 нм перемешаны с sp3–алмазными областями [21].
| |
 |
|
Рис. 5 TEM — изображение и соответствующая ему модель структуры стекловидного углерода, показывающая взаимное врастание алмазоподобных и графитоподобных областей на 1 нм, Нода и Инагаки [21].
|
Позже мы увидим, что оправданность такой аргументации "по аналогии" теперь несомненно доказана. То, что в устойчивой жидкой воде существуют различные структуры, отчетливо показано экспериментами Кавамото и др. с использованием точно такого же подхода с равновесием в P—T пространстве, но уже для самой воды (см. рис. 6) [22].
Обратимся теперь к очень близким кристаллографическим соотношениям в структурах кремнезема и воды, отмеченным Берналем и Фоулером уже в 1933 г. [23] Именно они предположили наличие трех "нано-областей" со структурами, аналогичными SiO2-кварцу и SiO2-тридимиту. Вейл, Марбоу и многие другие изучали структурное сходство между растворами в H2O и SiO2 [24] (cм. обзор Эйтеля [25]). Большинству читателей, интересующихся биологическими эффектами, неизвестно, что обычная вода очень легко образует (некристаллическое) стекло — например, при погружении эмульсии в жидкий N2. К сожалению, во многих последних работах по H2O-стеклу, видимо, выпущена из виду обширная литература по SiO2, который близок к воде как в форме кристаллов, так и стекла. Несмотря на дебаты, приведенные у Мазурина и Порай-Кошица, чистое кварцевое стекло считают тетраэдрически координированной переохлажденной жидкостью со структурой подобной воде (но намного более вязкой) (см., например, работы Патела и др., Коннерта и Карле, Роя; т.е., такое стекло SiO2 также состоит из областей с различной упаковкой или структурными элементами [11, 26, 27, 28]).
Прикладывая давления ≈200 кбар к SiO2-стеклу при комнатной температуре, Бриджмен и Саймон впервые установили, что SiO2-стекло легко может быть приготовлено и сохранено с двуми совершенно разными структурами при лабораторных давлениях и температурах [29]. Затем Коэн и Рой в серии работ четко доказали, что явление явного структурного изменения под воздействием давления — общее свойство фактически всех стекол с прочными связями [30—32]. Тридцать лет спустя, не зная, вероятно, о ранней работе, Энджелл и др., и Киффер подтверждают параллели между SiO2 и H2O с помощью данных для стекловидной воды; последний заявляет, что эти данные "серьезно поддерживают концепцию полиаморфизма, то есть наличия разных некристаллических структур в строении стекловидной воды" [3, 33]. Хотя такой "наногетерогенный" взгляд на воду и возможное "фазовое поведение метастабильной воды" с недавних пор появляются в литературе, возможность распространения на "стабильную воду" приведенных здесь данных — более ранних, очень обширных и значимых — малоизвестна и нигде не упоминается [34, 35]. Недавно Сопер, Талк и др., Де Бенедетти и Стэнли однозначно приняли концепцию наногетерогенности в стекловидной H2O [4, 36, 37]. Они также делают вывод, что в H2O-стекле есть разрывы и переходы первого порядка между "различными метастабильными формами" при превращении из одной в другую. Работа Кавамото и др. (см. рис. 6) показывает существование (пока лишь) двух "полиморфов" для устойчивой жидкой воды на P—T диаграмме, аналогичное обсуждавшимся выше диаграммам для S и др. [22]. Это явление возникает не в стекловидной или метастабильной, а в стабильной жидкой воде. Таким образом, они приходят к тому же самому заключению (путем точно такого же анализа P-T равновесия), которое мы сделали на основе вышеприведенных данных по P-T диаграммам S, Se, Te, и др.: наличие разных кристаллических структур — отличный намек на возможные различия в структурах жидкости.
| |
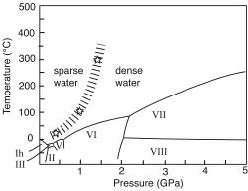 |
Рис. 6 Работа Кавамото и др. показывает области существования по крайней мере двух структур в области стабильной жидкой воды, полностью аналогично экспериментальным данным, полученным 35 годами ранее [22] для нескольких жидких структур в жидкой сере
на рис. 4.
|
Можно подытожить важность этих данных по термодинамике жидкой воды, последовавших за более ранними исследованиями S, Se, Te и др., хотя они, возможно, неочевидны для незнакомых с этим направлением термодинамики. В обычной термодинамике (как ясно из любого учебника по фазовым диаграммам) в стабильной области газа и моножидкости фиксированного состава может быть только одна фаза, в отличие от твердых веществ, где можно найти даже дюжину фаз. При фиксированном составе нет фазовых переходов "жидкость A ↔ жидкость B". Следовательно, эти данные — обширные ранние работы и теперь статья о воде — требуют основательного пересмотра прежнего мнения о структуре(ах) воды. Эти данные дают также несколько важных указаний относительно кинетики изменения таких структур. При традиционном подходе обычно используют аргумент, что если новые кластеры (или нано-"структуры") и формируются, то они должны быть очень нестойкими, т.к. время жизни связи может быть оценено как
| |
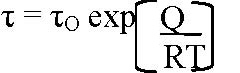 |
где τ0 — период колебаний (≈h/kT • 1,6 x 10-13с при комнатной температуре). Подстановка энергии типичных водородных связей дает время жизни средней одиночной водородной связи порядка микросекунды (для сильной ковалентной связи оно увеличивается до 106 и более лет). Однако это не то, о чем идет речь. Рассмотрим некоторые из больших олигомеров, содержащие около 200 молекул H2O, на которые ссылается вебсайт Мартина Чаплина (рис. 8 и 9) [38]. Они, по-видимому, не разрушаются полностью, а каждую микросекунду перестраиваются, разрывая некоторых общие связи. Фазовая диаграмма Кавамото и др. (рис. 6) доказывает, что по крайней мере за время эксперимента (минуты-часы) при определенных условиях P—T существуют структурно отличающиеся фазы с характерными свойствами, которые делают возможным обнаружение фазовой границы [22]. Точно так же сходство H2O с другими описанными жидкостями заключается не в идентичности их наиболее сильных ковалентных связей, а в вероятном подобии связей, соединяющие кластеры, поскольку они позволяют подробно изучить схожие фазовые изменения в одинаковом диапазоне P-T, с температурой в качестве основного фактора разрушения связей.
Интуитивно разумная концепция распространения структур из кристаллических фаз в жидкость послужила для Берналя основанием провести аналогию между H2O и SiO2 [23]. Коннерт и Карле однозначно идентифицировали в SiO2–стекле присутствие тридимитной структуры SiO2 [27]. Двухфазная модель воды Робинсона основана на существовании плотного и менее плотного льда, а недавно Бенедитти и Стэнли предположили, что фрагменты двух разных кристаллических структур льда должны сохраняться в области жидкой воды [4, 39]. Отметим, что соответствующая кинетика обеспечивает постоянство структурных элементов при условиях, близких к нормальным (кристаллическая форма определяет кластеры, области негетерогенности и т.п.). Абсолютно очевидно, что по крайней мере некоторые из них достаточно долговечны, поскольку они и задают отличительные свойства.
Обобщение фактических экспериментальных данных по структуре множества стекол и жидкостей, накопленных за 50 лет, показывает:
a. Вездесущность наномасштабной гетерогенности в структуре многих жидкостей с ковалентными связями.
b. Такая гетерогенность в нанометровом масштабе скорее правило, чем исключение для структуры всех жидкостей с прочными связями (т.е. в основном исключаются ионные и металлические расплавы).
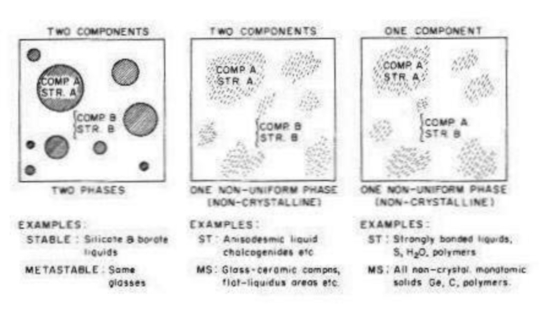
Рой в обзоре по структуре стекол и их нуклеации и кристаллизации [15] сделал вывод, что такая "наногетерогенность" — наиболее общая модель стекол. Рис. 7a, взятый из его работы (подтвержденный более поздними данными Мазурина и Порай-Кошица), представляет собой очень грубую схему, которая должна заменить в нашем сознании рис. 1 как более близкое приближение к действительности для "структуры жидкостей" (в основном с ковалентными связями) [11, 15].
| |
 |
|
Рис. 7a Схема Роя [15] более обобщенной структуры стекла, ясно указывающая ее гетерогенную природу (по отношению к структуре и/или составу). Заметьте, что в третьей колонке упомянута вода. Это новое минималистское схематическое представление структуры воды.
|
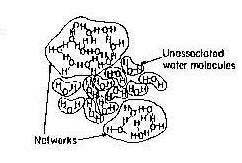
Поразительно похожа схема (рис. 7b) из учебника по электрохимии Бокриса и Редди [40].
| |
 |
|
Рис. 7b Похожее представление водной структуры Бокриса и Редди [40].
|
Жидкости, с которыми мы имеем дело, подобны H2O и состоят из статистически распределенных молекулярных агрегатов различного размера, структуры и (там, где это возможно) состава. Кроме того, точно установлено, что основные изменения таких структур (то есть расположение таких агрегатов или кластеров в пространстве) действительно оказываются функцией температуры и давления для всех обычных стекол (даже монотонных). Многие изменения тонкой структуры в этих стеклах остаются стабильными (т.е. демонстрируют своего рода память) в течение многих лет. Вслед за открытием Бриджмена и Саймона, в обширной работе Коэна и Роя было показано, что как для SiO2-стекла, так и для стекол всех исследованных составовплотность и показатель преломления, а следовательно и структура, были непрерывной функцией давления, и что такие твердые формы с высокой плотностью могли быть восстановлены и сохранялись в метастабильном состоянии в условиях комнатной температуры в течение многих лет [29–32].
Актуален вопрос о долговечности специфических структур, об их статистическом распределении и о статистическом распределении как функции температуры. Есть соответствующие данные, касающиеся этого вопроса, но не дающие количественных ответов — например, что концентрация разных кластеров или фрагментов, напоминающих "плотный лед", который должен присутствовать во всех образцах воды, при 30C или 40C намного выше, чем при комнатной температуре. И эти кластеры не исчезают из-за различных явлений, связанных с разрушением связей. Они, конечно, находятся в термодинамически стабильном равновесии (то есть сохраняются всегда).
ДАЛЕЕ
|

 Приветствую Вас Гость | RSS
Приветствую Вас Гость | RSS